Ornitin
| |

| |
| Adlandırmalar | |
|---|---|
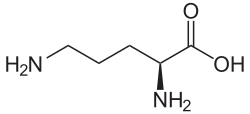
L-Ornitin | |
Diğer adlar (+)-(S)-2,5-Diaminovalerik asit (+)-(S)-2,5-Diaminopentanoik asit | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.665 |
| EC Numarası |
|
| KEGG | |
| MeSH | Ornithine |
PubChem CID
|
|
| UNII | |
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Molekül formülü | C5H12N2O2 |
| Molekül kütlesi | 132,16 g/mol |
| Erime noktası | 140 °C (284 °F; 413 K) |
| Çözünürlük (su içinde) | çözülebilir |
| Çözünürlük | etanolde çözülebilir |
| Asitlik (pKa) | 1,94 |
Kiral dönüş ([α]D)
|
+11,5 (H2O, c = 6,5) |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |
| Bilgi kutusu kaynakları | |
Ornitin, üre döngüsünde rol alan non-proteinojenik α-amino asittir. Radikal haline ornitil denir. Ornitin transkarmabilaz yetmezliğinde ornitin vücutta anormal şekilde birikir.[1]
Üre siklusundaki rolü
[değiştir | kaynağı değiştir]L-Ornitin, L-arjininin arjinaz enzimi ile katalizlenizlenmesiyle üre ile beraber oluşan üründür. Yani ornitin, vücuttaki fazla azotun atılmasını sağlayan üre döngüsünün, nam-ı diğer ornitin siklusu, merkezi bir parçasıdır. Bir nevi bir katalizatördür.
Önce amonyak karbomil fosfat sentetaz enzimi tarafından karbomil fosfata (H2NC(O)OPO2-3) dönüştürülür. Ardından ornitin transkarbamilaz enzimi, ornitin ve karbomil fosfat arasındaki reaksiyonu katalizleyerek sitrülin ve fosfat(Pi) oluşturur. Sonrasında aspartattan bir başka amino grubu daha alır ve arjinin ve denitronije fumarat oluşur. Ortaya çıkan arjinin (bir guanidinyum bileşiği) hidrolize olarak tekrardan ornitine dönüşür ve üre oluşur. Üreyi oluşturan amino grupları amonyak ve aspartattan gelir ve ornitindeki azotlar ise değişmeden kalır.

Ornitin DNA'da kodlanmamış bir amino asittir, yani proteinojenik değildir. Lakin memelilerin ekstrahepatik dokularında üre döngüsünün esas kullanım alanı arginin biyosentezidir ve bu sebeple metabolizmanın ara maddesi olarak ornitin önemlidir.[3]
Diğer reaksiyonları
[değiştir | kaynağı değiştir]Ornitin, ornitin dekarboksilaz (E.C. 4.1.1.17) sayesinde putresin gibi poliaminlerin sentezindeki başlagıç noktasıdır.
Bakterilerde, örneğin E.coli, ornitin L-glutamattan sentezlenebilir.[4]

Ayrıca bakınız
[değiştir | kaynağı değiştir]Kaynakça
[değiştir | kaynağı değiştir]- ^ Sivashanmugam, Muthukumaran; J., Jaidev; V., Umashankar; K.n., Sulochana (1 Şubat 2017). "Ornithine and its role in metabolic diseases: An appraisal". Biomedicine & Pharmacotherapy. 86: 185-194. doi:10.1016/j.biopha.2016.12.024. ISSN 0753-3322.
- ^ Langley, David B.; Templeton, Matthew D.; Fields, Barry A.; Mitchell, Robin E.; Collyer, Charles A. (30 Haziran 2000). "Mechanism of Inactivation of Ornithine Transcarbamoylase by N δ-(N′-Sulfodiaminophosphinyl)-l-ornithine, a True Transition State Analogue?: Crystal structure and implications for catalytic mechanism". Journal of Biological Chemistry (İngilizce). 275 (26): 20012-20019. doi:10.1074/jbc.M000585200. ISSN 0021-9258. PMID 10747936.
- ^ Weber, Arthur L.; Miller, Stanley L. (1 Eylül 1981). "Reasons for the occurrence of the twenty coded protein amino acids". Journal of Molecular Evolution (İngilizce). 17 (5): 273-284. doi:10.1007/BF01795749. ISSN 1432-1432.
- ^ "Ornithine Biosynthesis". iubmb.qmul.ac.uk. Erişim tarihi: 31 Mart 2025.
