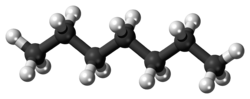
Heptan

| |
| |
| Adlandırmalar | |
|---|---|
Tercih edilen IUPAC adı Heptan[1] | |
Diğer adlar Septan[2] | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| 1730763 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.005.058 |
| EC Numarası |
|
| 49760 | |
| MeSH | n-heptane |
PubChem CID
|
|
| RTECS numarası |
|
| UNII | |
| UN numarası | 1206 |
CompTox Bilgi Panosu (EPA)
|
|
| |
| Özellikler | |
| Kimyasal formül | C7H16 |
| Molekül kütlesi | 100,20 g mol−1 |
| Görünüm | renksiz sıvı |
| Koku | benzin benzeri |
| Yoğunluk | 0.6795 g cm−3[3] |
| Erime noktası | [dönüştürme: geçersiz sayı] |
| Kaynama noktası | 9.838[3] °C (17.740 °F; 10.111 K) |
| Çözünürlük (su içinde) | 0.0003% (20 °C)[4] |
| log P | 4.274 |
| Buhar basıncı | 5.33 kPa (at 20.0 °C) |
Henry yasası
sabiti (kH) |
12 nmol Pa−1 kg−1 |
| −85.24·10−6 cm3/mol | |
| Kırınım dizimi (nD) | 1.3855[3] |
| Akmazlık | 0.389 mPa·s[5] |
| Dipol momenti | 0.0 D |
| Termokimya | |
Isı sığası (C)
|
224.64 J K−1 mol−1 |
Standart molar entropi (S⦵298)
|
328.57 J K−1 mol−1 |
Standart formasyon entalpisi (ΔfH⦵298)
|
−225.2 – −223.6 kJ mol−1 |
Standart yanma entalpisi (ΔcH⦵298)
|
−4.825 – −4.809 MJ mol−1 |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar |    
|
| İşaret sözcüğü | DANGER |
| Tehlike ifadeleri | H225, H304, H315, H336, H410 |
| Önlem ifadeleri | P210, P261, P273, P301+P310, P331 |
| NFPA 704 (yangın karosu) |
|
| Parlama noktası | [dönüştürme: geçersiz sayı] |
| 2.230 °C (4.050 °F; 2.500 K) | |
| Patlama sınırları | 1.05–6.7% |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LC50 (medyan konsantrasyon)
|
17,986 ppm (fare, 2 saat)[6] |
LCLo (yayınlanan en düşük)
|
16,000 ppm (insan) 15,000 ppm (fare, 30 dk)[6] |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | TWA 500 ppm (2000 mg/m3)[4] |
| REL (tavsiye edilen) | TWA 85 ppm (350 mg/m3) C 440 ppm (1800 mg/m3) [15-minute][4] |
| IDLH (anında tehlike) | 750 ppm[4] |
| Benzeyen bileşikler | |
Benzeyen alkanlar
|
|
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
n-Heptan (C7H16), alkanlar sınıfından doymuş bir hidrokarbondur. Oda sıcaklığında sıvı hâldedir. Çözücü olarak sanayi ve laboratuvarlarda kullanılır. Yanıcıdır.
Kullanımları
[değiştir | kaynağı değiştir]Heptan ve birçok izomeri laboratuvarlarda apolar çözücüler olarak yaygın şekilde kullanılmaktadır. Sıvı olduğundan taşınması ve depolanması kolaydır.
Heptan ayrıca pul koleksiyoncuları tarafından yapışkan sökücü olarak da kullanılır.
Sulu brom, sulu iyottan heptan içerisine ekstraksiyon sonrasındaki görünümüyle ayırt edilebilir. Suda hem brom hem de iyot kahverengi görünür. Bununla birlikte, iyot heptan içinde çözündüğünde mora dönerken, brom çözeltisi kahverengi kalır.
Sağlık etkileri
[değiştir | kaynağı değiştir]Heptan buharlarına akut maruziyet, baş dönmesine, uyuşukluğa, koordinasyon bozukluğuna, iştah kaybına, mide bulantısına, dermatite, kimyasal pnömoniye, bilinç kaybına veya olası periferik nöropatiye neden olabilir.[7]
Bir CDC çalışmasında, heptana uzun süre maruziyetin bazı çalışanlarda rehavete ve sarhoşluğa, yakındaki kişilerde ise maruziyetten sonra 30 dakika süren sersemliğe neden olabileceği bulunmuştur.[8]
İzomerleri
[değiştir | kaynağı değiştir]Heptanın dokuz tane izomeri vardır.
- Heptan (n-heptan), H3C–CH2–CH2–CH2–CH2–CH2–CH3
- 2-Metilhekzan (izoheptan), H3C–CH(CH3)–CH2–CH2–CH2–CH3
- 3-Metilhekzan, H3C–CH2–C*H(CH3)–CH2–CH2–CH3 (kiral)
- 2,2-Dimetilpentan, (H3C)3–C–CH2–CH2–CH3
- 2,3-Dimetilpentan, (H3C)2–CH–C*H(CH3)–CH2–CH3 (kiral)
- 2,4-Dimetilpentan, (H3C)2–CH–CH2–CH–(CH3)2
- 3,3-Dimetilpentan, H3C–CH2–C(CH3)2–CH2–CH3
- 3-Etilpentan, H3C–CH2–CH(CH2CH3)–CH2–CH3
- 2,2,3-Trimetilbütan, CH3–C(CH3)2–CH(CH3)–CH3
Kaynakça
[değiştir | kaynağı değiştir]| Organik kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |
- ^ "n-heptane – Compound Summary". PubChem Compound. Identification and Related Records: National Center for Biotechnology Information. 16 Eylül 2004. 23 Ekim 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Ocak 2012.
- ^ Hofmann, August Wilhelm Von (1 Ocak 1867). "I. On the action of trichloride of phosphorus on the salts of the aromatic monamines". Proceedings of the Royal Society of London. 15: 54-62. doi:10.1098/rspl.1866.0018.
- ^ a b c d Haynes, William M., (Ed.) (2011). CRC Handbook of Chemistry and Physics (92. bas.). Boca Raton, FL: CRC Press. s. 3.290. ISBN 1-4398-5511-0.
- ^ a b c d NIOSH Pocket Guide to Chemical Hazards. "#0312". Ulusal İş Güvenliği ve Sağlığı Enstitüsü (NIOSH).
- ^ Dymond, J. H.; Oye, H. A. (1994). "Viscosity of Selected Liquid n-Alkanes". Journal of Physical and Chemical Reference Data. 23 (1): 41-53. Bibcode:1994JPCRD..23...41D. doi:10.1063/1.555943. ISSN 0047-2689.
- ^ a b "n-Heptane". Immediately Dangerous to Life or Health Concentrations (IDLH). Ulusal İş Güvenliği ve Sağlığı Enstitüsü (NIOSH).
- ^ Patty, FA; Yant, WP (1929). "Odor intensity and symptoms produced by commercial propane, butane, pentane, hexane, and heptane vapor". Report of Investigations. US Department of Commerce, U.S. Bureau of Mines. No. 2979 (December): 1-10. 28 Ocak 2024 tarihinde kaynağından arşivlendi23 Mart 2024.
- ^ "CDC - Immediately Dangerous to Life or Health Concentrations (IDLH): n-Heptane - NIOSH Publications and Products". www.cdc.gov (İngilizce). 2 Kasım 2018. 25 Ekim 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Aralık 2021.

